
Sommaire
AVERTISSEMENT
Cet article a près de 10 ans. Certaines informations scientifiques ou médicales ont peut-être évolué avec des changements significatifs dans les interprétations et recommandations. N’hésitez pas à vous référer à des articles plus récents sur ce sujet.
Suite de la polémique sur la vaccination contre les Papillomavirus
Dans un article précédent, je vous ai exposé la polémique qui sévit actuellement contre les vaccins HPV (Human Papilloma Virus), mais surtout contre le dernier rapport émis par le Haut Conseil de Santé Publique (HCSP) qui recommande une vaccination dès 9 ans à l’école.
Dans cet article en date du 3 novembre, vous appreniez que le rapport émis par l’HCSP présentait les « données actualisées » sur l’efficacité et l’innocuité des deux vaccins, Gardasil et Cervarix, sur la base de nombreuses études scientifiques.
Malheureusement, je vous ai démontré que l’analyse de la sécurité des vaccins, détaillée sur 3 pages avec 9 références scientifiques, n’était absolument pas indépendante.
Ainsi, les 13 experts à l’origine de cette saisine, dont 5 affichent des liens d’intérêts avec les labos pharmaceutiques qui produisent et/ou commercialisent des vaccins HPV, ont choisi 9 études non indépendantes, bien souvent commanditées et payées par ces mêmes labos.
Comment peut-on croire à l’innocuité de ces vaccins dès lors que les labos pharmaceutiques apportent eux-mêmes les preuves de cette soit-disant innocuité ?
Je pose cette question aux 13 membres à l’origine de cette saisine, mais également aux deux comités compétents en la matière, qui ont validé ce rapport, et dont 2/3 tiers des membres possèdent des liens d’intérêts avec GSK, Sanofi-Pasteur MSD ou Merck.
Quoi qu’il en soit, je vous propose aujourd’hui de découvrir une analyse plus approfondie du rapport de l’HCSP sur les vaccins HPV.
Les vaccins Gardasil et Cervarix sont-ils efficaces contre les HPV ?
Nous allons nous pencher en détail sur un paragraphe précis et majeur du rapport :
« 1.2 – Impact sur la prévalence de l’infection HPV »
Ce paragraphe de la saisine du Haut conseil de la santé publique est majeur car c’est bien lui qui justifie l’utilisation des vaccins Gardasil et Cervarix contre les infections HPV, et donc hypothétiquement contre le cancer du col de l’utérus.
Les experts à l’origine de cette saisine ont choisi 6 références scientifiques qui ont étudié l’effet des vaccins cités sur la prévalence (la fréquence d’apparition) des différentes souches de papillomavirus.
Les experts ont choisi de détailler 3 études, et d’en citer 3 autres brièvement au début du paragraphe.
Nous allons revenir en détail sur ces 6 références, en épluchant :
- La méthodologie employée
- Les limitations qui en découlent
- Les résultats significatifs et non significatifs
- Les conflits d’intérêts
Vous allez découvrir que toutes les études citées ne sont pas indépendantes, que les méthodes employées entraînent des biais importants, et que certains résultats non significatifs ne sont tout simplement pas mentionnés.
Les 3 études mises en avant par l’HCSP
Analyse étude par étude.
Première étude américaine
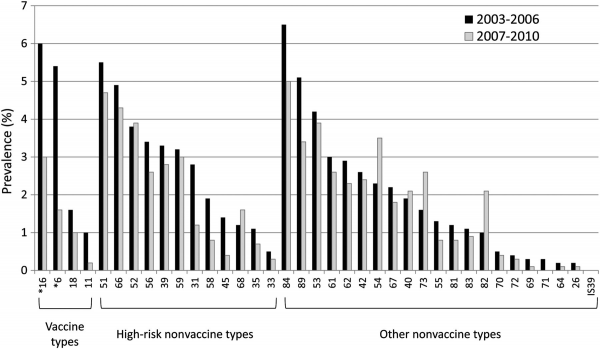
D’après la saisine de l’HCSP, « la prévalence des HPV vaccinaux a diminué de 11,5% à 5,1% (-56%) parmi les jeunes filles de 14-19 ans […] »
Les experts précisent « qu’il n’y a pas eu de diminution observée dans d’autres groupes d’âge. »
En effet, si l’on regarde les tableaux fournis par les scientifiques, la fréquence d’apparition des quatre génotypes auraient été réduite de moitié après la vaccination.
Les experts précisent également que le vaccin n’a eu aucun effet sur les autres groupes d’âge, tous les autres !
Ainsi, il n’y a eu aucun changement significatif de la prévalence des HPV chez les 20-24 ans, les 25-29 ans, les 30-39 ans, les 40-40 ans et les 50-59 ans.
Plus intéressant encore, les experts de la saisine ne mentionnent pas le fait que seule la prévalence de 2 souches sur les 4 visées par le Gardasil ont effectivement diminué.
Le graphique ci-dessus vous présente ces résultats. Ainsi, nous voyons en réalité que seul le génotype 16, à risque, et le 6, à faible risque, ont une prévalence plus faible après la vaccination. Le deuxième génotype à risque, le 18, qui n’avait qu’une prévalence de 1,5% n’a statistiquement pas changé (aucune astérisque noire).
Le génotype 6 jugé à faible risque oncogène (donc promoteur d’un cancer) observe une forte diminution de sa prévalence (de 5,3% à 1,6%) mais c’est bien le génotype 18 qui nous intéresses.
Pour le génotype 18, la prévalence dans l’échantillon est faible. Seulement 6%. L’étude nous montre qu’après la vaccination au Gardasil (contre les 4 souches) la prévalence de ce dernier n’est plus que de 3%, soit une baisse de 50%.
L’analyse fine de cette étude nous montre que les résultats ne sont pas si exceptionnels qu’il n’y paraît.
Sur les quatre génotypes censés être limités par le Gardasil, seulement deux le sont réellement, parmi lesquels un seul à haut risque, et de surcroît, dans une seule classe d’âge sur 6 !
Voilà pourquoi les experts de l’HCSP classe ce niveau de preuve comme une présomption scientifique (niveau 2).
Par ailleurs, cette étude présente de nombreuses limitations assumées et détaillées par les auteurs de la recherche.
Premièrement, le statut sur la vaccination des patients recrutés a été réalisé par les patients eux-mêmes, avec des questionnaires. Selon les auteurs, cela pourrait conduire à des « surestimations ou des sous-estimations » de la vaccination. Les auteurs le disent eux-mêmes :
« Il est probable qu’il y ait eu des erreurs de classification dans le statut vaccinale de l’étude Nhanes, qui auraient pu biaisé nos analyses et nos estimations de l’efficacité du vaccin ».
Une efficacité, qui je vous le rappelle, a été estimée à 82% par les auteurs.
Deuxièmement, les auteurs admettent que la base de données qu’ils ont utilisé (Nhanes) ne leur permet pas de faire des estimations spécifiques de prévalence.
Troisièmement, les auteurs affirment qu’une nouvelle méthode d’échantillonnage a été choisi en cours de route pour recueillir les participantes.
Finalement, les scientifiques concluent que « quelqu’une de leurs analyses ont été limitées par la taille de l’échantillon, et que quelques estimations de prévalence [pour les génotypes] étaient instables. »
Pour terminer, et c’est une bonne nouvelle qu’il faut souligner, l’étude est indépendante.
Référence:
Markowitz LE, Hariri S, Lin C, Dunne EF, Steinau M, McQuillan G, Unger ER. Reduction in human papillomavirus (HPV) prevalence among young women following HPV vaccine introduction in the United States, National Health and Nutrition Examination Surveys, 2003-2010. J Infect Dis. 2013; 208(3): 385-93
Deuxième étude australienne
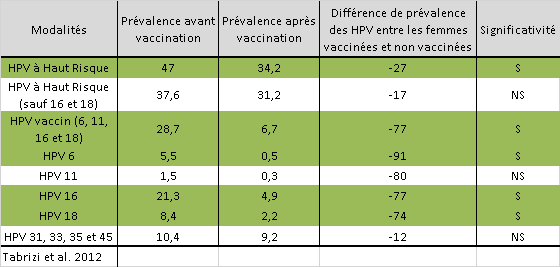
Cette étude publiée en 2012 nous indique une baisse record de la prévalence des génotypes vaccinaux (encore sur le Gardasil) 6, 11, 16 et 18, passant de 28,7% à 6,7% en post-vaccination.
Sur les 6 études sélectionnées par le groupe de travail de l’HCSP, celle-ci nous montre les résultats les plus encourageants et les plus impressionnants quant à l’efficacité du vaccin sur la prévalence des génotypes visés.
Il est tout de même bon de mentionner que le génotype 11 n’a montré aucune différence significative de prévalence (NS) avant et après l’événement de vaccination.
Dans cette étude, il est intéressant de préciser que les auteurs ne mentionnent aucune limitation ou biais présent dans l’étude, comme il est pourtant habituel de le faire.
Il est d’autant plus intéressant de mentionner, contrairement aux experts de l’HCSP, que 5 auteurs sur 10 ont des liens d’intérêts majeurs avec l’industrie pharmaceutique en charge de la fabrication et de la revente de vaccins HPV.
Voici la liste des auteurs, par ordre d’apparition dans la publication et donc par ordre d’importance, et l’ensemble des liens d’intérêts déclaré.
Vous devez savoir que la première et la dernière place dans une publication sur les plus importantes. La première place indique l’auteur ayant le plus contribué à la recherche, et la dernière place revient en général au directeur du laboratoire de recherche, une position largement favorable pour orienter une étude dans un sens ou dans un autre.
Conflits d’intérêts:
- Sepehr N. Tabrizi: Ce scientifique a reçu des « financements illimités » de la part de GSK et CSL Biotherapies pour faire des études scientifiques similaires. GSK et CSL Biotherapies commercialisent des vaccins HPV.
- Julia M. L. Brotherton: Cette chercheuse a également reçu des « financements illimités » de la part de GSK et CSL Biotherapies pour faire des études du même type. Elle fait également parti d’un comité de recherche en partie financé par CLS Biotherapies.
- John M. Kaldor: Sans conflit d’intérêt.
- Rachel Skinner: Elle a été l’investigatrice de nombreux essais cliniques sur les vaccins HPV financés par GSK. Son institution de recherche a reçu des fonds pour collecter des données pour GSK. Son institution a également reçu des honoraires pour avoir participé à des comités de conseil de GSK. Les déplacements et les frais de participations lors de congrès afin de présenter les résultats de GSK Biological ont été remboursés par GSK Biological. Finalement, son institution a reçu des financements illimités de la part de GSK Australia et CSL Biotherapies.
- Eleanor Cummins: Sans conflit d’intérêt
- Bette Liu: Elle possède des actions dans une société qui vend des vaccins HPV (le Commonwealth Serum Laboratories)
- Deborah Bateson: Sans conflit d’intérêt
- Kathleen McNamee: Sans conflit d’intérêt
- Maria Garefalakis : Sans conflit d’intérêt
- Suzanne M. Garland: Cette scientifique a reçu des compensations financières de CSL Biotherapies et GSK lors de participations à des comités de conseil. Elle a également reçu des honoraires de Merck en tant que conférencière et consultante. Elle possède aussi des actions dans la société CSL Biotherapies qui revend des vaccins HPV. Elle a reçu des fonds de la part de Merck et GSK pour réaliser des études cliniques sur les HPV et sur le cancer du col de l’utérus. Elle est également membre du comité global et scientifique détenu par Merck.
A la lumière de ces liens d’intérêts majeurs, il convient de prendre avec des pincettes l’efficacité du vaccin testé dans cette étude, qui plus est, n’est classé qu’en tant que présomption scientifique (niveau de preuve n°2).
Référence:
Tabrizi SN, Brotherton JM, Kaldor JM, Skinner SR, Cummins E, Liu B, Bateson D, McNamee K, Garefalakis M, Garland SM. Fall in human papillomavirus prevalence following a national vaccination program. J Infect Dis. 2012; 206(11): 1645-51.
3ème étude britannique
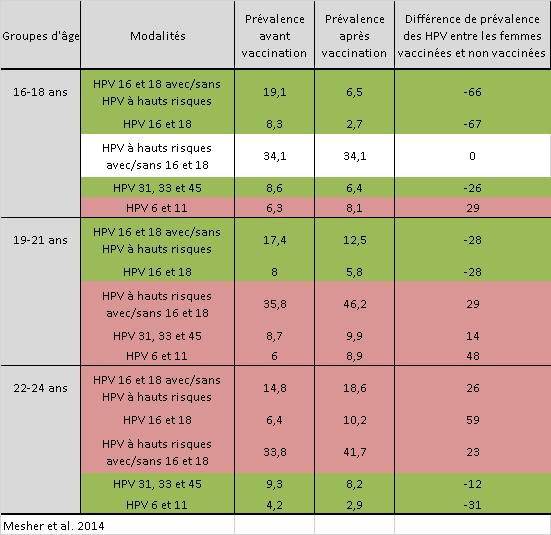
Finalement, la dernière étude détaillée dans ce paragraphe « impact sur la prévalence de l’infection HPV », nous indique que « la prévalence des HPV vaccinaux (16 et 18) chez les jeunes filles âgées de 16-18 ans a diminué de 19,1% en 2008 à 6,5% en 2010-2012 […] ».
C’est tout à fait exact, la baisse étant de l’ordre de 66%.
Vous pouvez remarquer que les auteurs du rapport n’ont en réalité cité que la première ligne du tableau des résultats, que j’ai simplifié pour vous.
Le vert indiquant toujours une baisse de la prévalence après la vaccination, le rouge l’inverse.
Tout d’abord, il est intéressant de remarquer que cette baisse de 12,6 point (-66%) n’est pas strictement limitée aux génotypes 16 et 18.
En effet, la première ligne indique bien que ces résultats de prévalence sont calculés pour nos génotypes cibles (16 et 18) mais également avec ou sans, on ne sait pas trop, d’autres génotype à risque.
En réalité, cette première ligne établit la prévalence d’au moins 11 génotypes, 13 au maximum, mais encore une fois, nous n’en savons rien.
C’est bien la seconde ligne de ce tableau qui nous indique l’effet de la vaccination sur nos deux génotypes ciblés (16 et 18) et nous observons bien une baisse de la prévalence de ces deux HPV à haut risque.
Cependant, la prévalence de ces deux génotypes apparait faible dans l’échantillon, avec seulement 8,3% des jeunes filles de 16-18 ans échantillonnées.
Quoi qu’il en soit, les experts de l’HCSP ont omis de mentionner l’ensemble des lignes rouges, qui représentent des augmentations de la prévalence des génotypes HPV, et donc des risques potentiels, si j’en crois les laboratoires pharmaceutiques.
Le plus grave se trouve chez les 22-24 ans où tous les génotypes à risques (16, et 18 et les 11 autres à risques) augmentent après l’événement de vaccination.
Plus grave, les génotypes 16 et 18 augmente de près de 60% chez les jeunes filles de 22-24 ans, passant de 6,4% à 10,2%.
Ces résultats, inconsistant au sein des différents groupes d’âge, doivent nous alerter sur la qualité de l’échantillonnage, de la méthodologie, des analyses et des interprétations que l’on peut en tirer.
Cette étude a été classé selon l’HCSP en catégorie 2, soit seulement des présomptions scientifiques (autant valables pour les aspects positifs que négatifs).
Finalement, cette étude est indépendante, tant au niveau des financements que des auteurs de la recherche.
Références:
Mesher D, Soldan K, Howell-Jones R, Panwar K, Manyenga P, Jit M, Beddows S, Gill ON. Reduction in HPV 16/18 prevalence in sexually active young women following the introduction of HPV immunisation in England. Vaccine 2013; 32(1): 26-32.
Les 3 études scientifiques non détaillés dans le rapport de l’HCSP
Maintenant je vais vous détailler les 3 autres études citées, mais non détaillées, par les experts de l’HCSP.
Pourquoi ces études n’ont été que citées ? Nous allons voir ça immédiatement.
4ème étude, non détaillée dans la saisine de l’HCSP
Cette étude a été mentionnée dans le rapport émis par le groupe de travail de l’HCSP mais non détaillée.
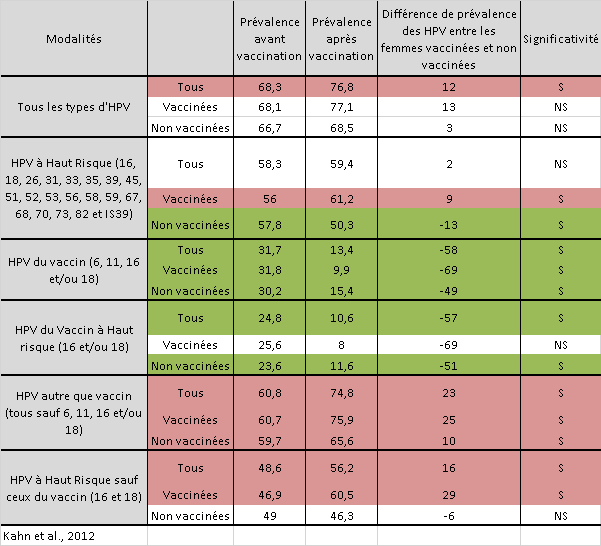
Toujours de la même manière, les lignes colorées indiquent les résultats significatifs (c’est-à-dire que les différences sont vraies et prouvées statistiquement) avec le rouge pour une prévalence augmentée et en vert quand elle diminue.
La première ligne peut attirer votre attention. De manière globale, la prévalence de tous les HPV augmente dans l’échantillon visé. L’augmentation est toutefois faible, seulement 12%.
La suite de ces résultats, c’est du mi-figue mi-raisin.
En effet, nous observons bien une baisse de la prévalence des HPV vaccinaux (de 49 à 69% de baisse), avec les 3 lignes vertes.
Encore plus intéressant, les résultats de prévalence pour les deux génotypes à hauts risques (16 et 18) affichent une prévalence en baisse chez les « Tous », vaccinées et non vaccinées compris.
C’est le but recherché du vaccin, on est donc ravis d’observer ce résultat.
En revanche, et ce sont les aléas du traitement statistique, la population vaccinée par le quadrivalent qui affiche une prévalence en chute libre de 25,6 à 8% (la ligne blanche) n’est pas statistiquement significative.
Cela veut dire que la taille de l’échantillon ou d’autres facteurs ne nous permettent pas de dire qu’il y a une différence avant et après vaccination.
Cette ligne blanche signifie donc que le vaccin Gardasil qui agit sur les génotypes 6, 11, 16 et 18 n’aurait eu aucun effet sur la prévalence des infections de ces 4 génotypes.
Les résultats sont quelque peu étranges, mais j’ai vérifié au moins 3 fois pour en être sûr !
La suite et la fin du tableau ne présente que des lignes rouges ou presque, avec donc une augmentation de la prévalence des certains génotypes dont certains à risques, et seraient notamment mis en cause dans 20 à 30% des cas de cancer du col de l’utérus.
Par ailleurs, les auteurs de cette étude dédient un long paragraphe sur les limitations inhérentes à leurs travaux.
Les scientifiques nous indiquent que l’échantillonnage de l’étude a changé lors de la phase pré et post-surveillance, pouvant entraîner des modifications sur la prévalence des HPV étudiées.
Egalement mis en avant dans cette étude, les auteurs n’excluent pas des erreurs dans le choix des participantes, et notamment sur le statut « vacciné ou non », qui était parfois manquant des registres.
Finalement, cette étude n’est malheureusement pas exempte de conflits d’intérêts. De la même manière que pour les études précédentes, voici la liste détaillée des conflits d’intérêts des auteurs par ordre d’apparition (et donc d’importance, sauf pour le dernier) dans la publication.
Ainsi, sur les 7 auteurs de cette étude, 3 dont les 2 premiers présentent des liens d’intérêts avec les labos pharmaceutiques en charge de vendre ou produire des vaccins HPV.
Conflits d’intérêts:
- Jessica A. Kahn: Elle est la co-dirigeante de deux essais cliniques sur des vaccins HPV dont Merck a assuré le stock de vaccins et les tests immunogénicités. Elle a également reçu des fonds de la part d’une société (SAHM), dont le financement a été assuré par Merck, pour assurer la présidence d’un comité d’évaluation de projets médicaux.
- Darron R. Brown: Ce scientifique fait partie du comité de conseil sur la santé des femmes de Merck, et son laboratoire reçoit des fonds de la part de Merck. L’université d’Indiana et Merck ont signé un contrat confidentiel qui rémunère l’Université en contre partie du développement d’un vaccin HPV en particulier, le docteur reçoit une partie de cette rémunération en tant que revenu financier.
- Lili Ding: Sans conflit d’intérêt
- Lea E. Widdice: Sans conflit d’intérêt
- Marcia L. Shew: Cette scientifique est l’investigatrice principale d’essai clinique sur les vaccins HPV dont le soutien financier est assuré par Merck.
- Susan Glynn: Sans conflit d’intérêt
- David I. Bernstein: Sans conflit d’intérêt
Finalement, cette étude présente des limitations (comme toutes les études scientifiques), des conflits d’intérêts et des résultats parfois contradictoires.
On comprend facilement pourquoi les experts n’ont pas détaillé cette étude, et l’on peut décemment se poser la question du risque de cette vaccination sur l’augmentation de la prévalence d’autres HPV (que le 16 et 18) dans la population.
Référence:
Kahn JA, Brown DR, Ding L, Widdice LE, Shew ML, Glynn S, Bernstein DI. Vaccine-type human papillomavirus and evidence of herd protection after vaccine introduction. Pediatrics. 2012; 130(2): e249-56.
5ème étude non détaillée par l’HCSP
Cette 5ème étude présente beaucoup moins de résultats que la précédente.
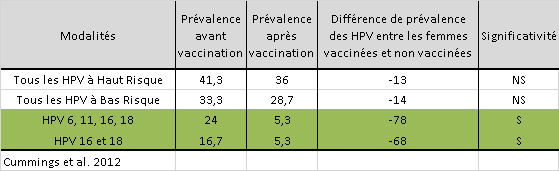
Ainsi, les deux résultats significatifs nous indiquent que la prévalence des HPV vaccinaux (6, 11, 16 et 18) diminue de 24% à 5,3% après la vaccination, soit une baisse de 78%.
Nous observons des chiffres relativement similaires pour les deux génotypes à hauts risques (16 et 18) avec toutefois un niveau de prévalence déjà bas (seulement 16,7%) avant la vaccination.
Au niveau des HPV à hauts risques, toutes les souches, aucune différence n’a été observé (première ligne). Idem pour les HPV à bas risque oncogène.
Au niveau des limitations, les auteurs en parlent en ces termes :
« La limitation la plus forte de l’étude était la séparation temporelle des deux cohortes (presque 10 ans) et donc nous ne pouvons pas exclure la possibilité que d’autres facteurs extérieurs non pris en compte ont contribué aux résultats sur la baisse des HPV détectées […] »
Autrement dit, les chercheurs admettent que le vaccin quadrivalent n’est peut-être pas le seul responsable de la baisse de la prévalence observée.
Cette étude n’est également pas épargnée par quelques conflits d’intérêts. Voici la liste, qui vous montre que 3 des 7 auteurs ont des liens avec les labos considérés.
Conflits d’intérêts:
- Teresa Cummings: Sans conflit d’intérêt
- Gregory D Zimet: Ce scientifique est l’investigateur de nombreux programmes de recherches financés par Merck.
- Darron Brown: Ce scientifique fait partie du comité de conseil sur la santé des femmes de Merck, et son laboratoire reçoit des fonds de la part de Merck. L’université d’Indiana et Merck ont signé un contrat confidentiel qui rémunère l’Université en contre partie du développement d’un vaccin HPV en particulier, le docteur reçoit une partie de cette rémunération en tant que revenu financier.
- Wanzhu Tu: Sans conflit d’intérêt
- Ziyi Yang: Sans conflit d’intérêt
- Dennis Fortenberry: Sans conflit d’intérêt
- Marcia L Shew: Investigatrice clinique de Merck pour des études sur les vaccins HPV.
Référence:
Cummings T, Zimet GD, Brown D, Tu W, Yang Z, Fortenberry JD, Shew ML. Reduction of HPV infections through vaccination among at-risk urban adolescents. Vaccine. 2012; 30(37): 5496-99.
6ème et dernière étude non détaillée
On va faire simple et court.
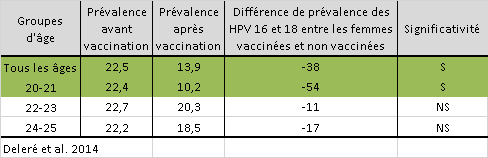
Les auteurs de cette étude ont observé la prévalence des génotypes à haut risque 16 et 18 sur un échantillon de jeunes filles, classées dans 3 groupes d’âge (20-21, 22-23 et 24-25 ans).
Comme vous pouvez le voir, un effet bénéfique de la vaccination n’a été observé que chez les 20-21 ans, avec une baisse de 22,4% à 10,2%.
Chez les 22-23 ans et les 24-25 ans, la vaccination ne montre aucun effet sur la prévalence de ces deux HPV à hauts risques.
Pour être complet, sur les 8 auteurs de l’étude, le dernier, Andreas Kaufmann, présente des conflits d’intérêts. Il a été expert et membre de comité pour GSK et Gen probe. Il a reçu des honoraires en tant que conférencier par Sanofi Pasteur MSD, GSK et Roche.
Référence:
Deleré Y, Remschmidt C, Leuschner J, Schuster M, Fesenfeld M, Schneider A, Wichmann O, Kaufmann AM. Human Papillomavirus prevalence and probable first effects of vaccination in 20 to 25 year-old women in Germany: a population-based cross-sectional study via home-based self-sampling. BMC Infect Dis. 2014; 14:87.
Au final, qu’est-ce que nous avons ? Faut-il oui ou non se faire vacciner ?
Après se déballage un peu rébarbatif sur ces études scientifiques, force est de constater certains points majeurs soulevés :
- Les conflits d’intérêts sont toujours présents dans la plupart des études sélectionnés, mais il convient de saluer le choix de certaines études complètement indépendante
- Les résultats des études sur la prévalence des HPV ne sont pas consistant : un coup ça monte, un coup ça descend, un autre coup c’est significatif et après ça ne l’est plus.
- La plupart des études présentent des biais sérieux qui ont peut-être modifié (positivement ou négativement) la prévalence des HPV testées.
- Si la plupart des résultats montrent une baisse de la prévalence des génotypes 16 et 18, on observe également une augmentation d’autres HPV à haut risque après la vaccination.
Au-delà de ces points, nous sommes en droit de nous demander…
Mais ça veut dire quoi 50% d’infections en moins après vaccination ?
Oui, concrêtement, quels seraient les impacts d’une baisse de 10 ou de 80% de la prévalence des HPV au sein de la population ?
Allons-nous réellement observer une baisse de l’apparition des cancers du col de l’utérus ?
Selon les labos, c’est oui. Mais selon moi, rien n’est moins sûr, et quand bien même cela arriverait réellement, quel en est le coût pour la société ?
Les probabilités d’avoir un cancer du col de l’utérus
Alors attention, dans ce parapraphe je vais oser me lancer des calculs probabilistes sur l’apparition d’un cancer du col de l’utérus. Je vais utiliser les données publiées, celles choisies par nos experts, mais également des probabilités issues du livre « Traité des infections et pathologies génitales à papillomavirus » par Joseph Monsonego.
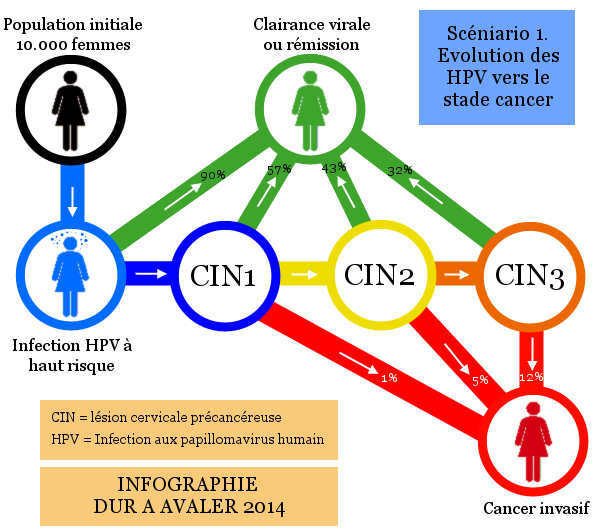
Voici l’évolution en image d’une infection aux HPV vers un état grave de cancer invasif.
Comme vous pouvez le voir, après avoir été infecté par un papillomavirus, vous avez des stades d’agravations de la maladie, dit CIN (de 1 à 3), pour terminer vers le stade cancer.
Avant d’en arrriver au stade cancer, tous les stades précédents possèdent une probabilité de rémission, et qui n’est pas faible.
Ces probabilités de rémission (ou de clairance virale comme on dit dans le jargon) varient de 32 à 57%.
Et vous devez également savoir que les infections HPV disparaissent fortement chez les personnes infectées.
Ainsi, le professeur Duport nous indique dans son chapitre dédié que « 70% des infections dispairassent en 12 mois et 90% en 24 mois ».
Ces chiffres de rémission ou de clairance virale s’appliquent pour tous les génotypes à hauts risques, et pas seulement les 16 et 18.
Je vais maintenant vous faire la démonstration par des calculs de probabilité, de quels sont les risques pour vous d’avoir un cancer du col de l’utérus, selon les chiffres de prévalence de l’étude australienne (avec de nombreux conflits d’intérêts) qui indique une baisse de 27% des HPV à hauts risques après vaccination.
Donc.
Je vais vous détailler la première série de calcul de probabilité, en imaginant que toutes les femmes passent par les 3 stades CIN avant le stade cancer.
Je vais également vous donner les résultats pour les deux autres scénarii : (1) toutes les femmes passent de l’infection au stade CIN2 et (2) toutes les femmes passent de l’infection au stade ultime CIN3 (cas extrême).
1er cas : Infection-CIN1-CIN2-CIN3-Cancer invasif
Sur 10.000 femmes, 47% d’entres-elles, ont un HPV à hauts risques, soit 4.700 femmes avec le virus.
Sur ces 4.700 femmes infectées, 90% d’entres-elles jouieront d’une clairance virale, soit 4.230 femmes sans infection, mais 470 femmes restants toujours infectés au stade CIN1.
Sur ces 470 femmes au stade CIN1, 57% d’entres-elles bénéficeront également d’une clairance virale, soit 268 femmes sauvées. Malheureusement, 5 femmes développeront un cancer invasif, 145 resteront à ce stade et 52 iront au stade CIN2.
Sur ces 52 femmes au stade CIN2, 43% retourne à la case départ «épithélium normal », tandis que 3 cancers invasifs apparaitront, 16 resteront à ce stade et 11 souffriront d’un stade CIN3.
Au stade CIN3, 1 femme sur 11 déclarera un cancer invasif, tandis que 4 s’en remettront et 7 demeureront à ce stade.
Au final, nous avons 9 cas de cancers du col de l’utérus.
Dans le scénario n°2, nous aurons 36 cas de cancers, et 56 cas dans le scénario le plus extrême n°3 (toujours selon le même procédé mathématique).
Maintenant, il est intéressant de noter l’évolution de ces cas de cancers théoriques avec l’efficacité des vaccins démontré scientifiquesment.
Je vous le rappelle, 27% de baisse de la prévalence des infectons HPV de hauts risques.
Ce qui nous donne après avoir vacciné 10.000 femmes :
- 2 cancers de moins pour le premier scénario
- 10 cancers de moins pour le second scénario
- 15 cancers de moins pour le dernier scénario
En terme de coût pour la santé publique, à 350 euros les 3 doses de Gardasil par exemple, cela revient à dépenser 1,75 millions d’euros pour éviter un cas de cancer, dont nous ignorons s’il entrainera la mort.
Dans le 2ème cas, le coût par cancer sauvé est de 350.000 euros, tandis qu’il est de 233.000 euros dans le dernier scénario.
Attention, je ne suis pas en train de dire qu’il ne faut pas prendre en compte ces cas graves de cancers du col de l’utérus. Je suis en train de replacer le tout dans son contexte, la priorité en terme de santé publique des autorités compétentes.
Est-ce que la mise en place d’un vaccin qui coûte cher, obligatoire à l’école, pour une maladie non épidémique qui se dépiste bien par les frottis est raisonnable ?
A cette question, je répond par la négative.
N’oublions également pas que sur les 10.000 femmes vaccinnées, et selon les statistiques internationales, deux d’entres-elles subiront des effets indésirables (ce qui est relativement peu, nous sommes d’accord).
Au final, et je rejoins l’avis de Martin Winckler sur ce sujet :
Vous n’avez mesdames aucun sentiment de culpabilité à avoir si vous ne vous faites pas vacciner contre les HPV.
Cela est également valable pour les mamans qui se posent des questions pour leurs filles.
A ce jour, les vaccins bivalents et quadrivalents contre les HPV ne protègent pas contre l’intégralité des infections à papillomavirus.
Nous n’avons pas le recul nécessaire pour mesurer l’efficacté réelle de ces vaccins sur la survenue des cancers du col.
Nous n’avons pas le recul nécessaire pour connaître l’efficacté de ce vaccin au-delà de 5 ans.
Nous n’avons pas le recul nécessaire pour connaître la totalité des effets secondaires liés à l’injection de ces vaccins.
Nous n’avons pas suffisamment de preuves scientifiques solides et totalement indépendantes.
En conclusion, force est de contaster que si le Gouvernement optait pour une vaccination obligatoire dans les écoles dès l’âge de 9 ans, cela serait un véritable scandale et absolument pas justifié.
Sur ce dernier point, je rejoins le combat de M. Joyeux.
N’oubliez pas qu’à partir de 25 ans, et jusqu’à 65 ans, un dépistage par frottis tous les 3 ans restent l’une des meilleures options pour lutter contre le cancer du col, 15ème cancer féminin sur le nombre de mort.

17 commentaires
Comme toujours, remarquable travail. Une précision supplémentaire, il n’échappera à personne qu’en France seuls trois vaccins sont obligatoires : ceux contre la diphtérie, le tétanos et la poliomyélite. Lorsqu’un rapport préconise l’introduction massive d’un vaccin dans une population donnée, il ne parle pas de le rendre obligatoire mais de le recommander.
L’intérêt ici n’est pas seulement terminologique : au nom de l’inviolabilité du corps humain (art. 16-1 c. civ.), toute personne est libre de refuser de se faire vacciner, tout comme de refuser un traitement ou une opération (c’est pourquoi je ne me suis pas fait vacciner contre la grippe aviaire)
Les seules dérogations étant accordées aux parents sur leurs enfants, au nom de l’autorité parentale, ainsi qu’à certaines professions pour lesquelles la vaccination contre certaines maladies est obligatoire (je pense ici aux professionnels de santé, en pédiatrie notamment).
Toute vaccination forcée est donc tout aussi improbable qu’elle serait contraire à la loi.
Oui, merci encore une fois pour cet article hyper intéressant…je transmets!
la survaccination…mais aussi les mammographies de dépistage systématique et les risques (prouvés) de surdiagnostic, sans parler de l’irradiation…avec les catastrophes que ça peut engendrer.
business…business…
c’est un autre sujet que j’aimerais bien que vous analysiez pour toutes les femmes qu’on culpabilise et qu’on maintient dans la peur et l’ignorance.
Vos recherches sur ce sujet seraient vraiment très profitable.
merci pour tout Jérémy. :)
Thanks for inritducong a little rationality into this debate.
Merci pour cet article encore une fois très documenté. Il est intéressant car il apporte une forte contribution à ce débat.
Belle étude ! Mon épouse, médecin scolaire, donc concernée pour une grande partie de ses “patientes”, est bien d’accord : vaccin inutile et hors de prix.
Une étude au bon moment… je me demandais justement si faire ou non vacciner ma fille. Ce sera donc non. Un si faible taux d’efficacité oblige á continuer d’employer les méthodes classiques de dépistage… donc le vaccin perd beaucoup de son intérêt.
A propos de l’étude de Markovitz :
il est normal qu’en dehors de la tranche d’âge des 14-19 ans, on n’observe rien de significatif. Le vaccin a été introduit en 2006 et l’étude porte sur la période 2007-2010 par rapport à la période 2003-2006. Les filles plus âgées n’ont tous simplement pas été vaccinées (sauf exceptions) (même topo pour l’étude 6 d’ailleurs, je suppose…). La variation relative de prévalence des HPV vaccinaux est donc de 56 % chez les 14-19 ans dans leur ensemble, vaccinées ou non (sachant que seules 34 % avaient reçus au moins une dose). Si on ne considère que les vaccinées, l’efficacité après au moins une dose est de 82 %. En ce qui concerne le HPV18, un résultat non significatif ne signifie pas forcément une absence d’effet. Il faut plutôt considérer (puisque les études préalables à la mise sur le marché ont montré un effet sur toutes les souches vaccinales) que si l’effet devait exister, il n’a pas pu être mis en évidence. Avec un couverture vaccinale de 34 % pour au moins 1 dose, et une proportion de 50 % de personnes sexuellement actives chez les 14-19 ans étudiées, il n’est pas surprenant qu’il soit difficile de mettre en évidence un effet sur des prévalences faibles, comme celle du HPV 18.
A propos de l’étude de Tabrizi :
Les auteurs bourrés de conflits d’intérêts mentionnent une efficacité de 73 %, donc moindre que dans le cadre de l’étude indépendante précédente qui concluait à 82 %. Est-ce qu’il faut en conclure qu’au plus les auteurs sont indépendants, au plus ils trouvent une efficacité élevée ? ;-)
A propos de Mesher :
Le « avec ou sans » est simplement lié à la possibilité d’être infectée par plusieurs génotypes en même temps. C’est donc bien la première ligne qui regroupe tous les cas où au moins 1 des deux génotypes 16 ou 18 a été détectés, et donc celle qui indique quelque chose sur l’efficacité du vaccin.
Si certains résultats du tableau ne valent pas la peine d’être discutés, c’est qu’il ne sont pas significatifs… par exemple, pour la première ligne des 22-24 ans, on trouve un OR de (0,9-2,00) dans l’article original. Bref, la valeur « neutre » d’un OR étant de 1, ce résultat n’était pas significatif. D’autres augmentations sont bien significatives au sens statistique, les auteurs en parlent et l’expliquent soit par un remplacement de souches vaccinales ou par les limitations de l’étude, mais sans pouvoir trancher.
A propos de l’étude de Kahn :
Même remarque que plus haut… ce n’est pas parce que l’effet n’est pas mis en évidence dans une étude possédant des limitations que cet effet n’existe pas… sauter à la conclusion qu’il n’y a aucun effet, sans tenir compte du contexte, des autres études, des connaissances préalables, etc.. c’est aller trop vite en besogne. Les augmentations de prévalence sont discutées par les auteurs, qui indiquent que seules les vaccinées sont concernées, et qu’il est tout à fait possible que les vaccinées (plus souvent des afro américaines sexuellement précoces ) n’ait pas le même profil de risque que les non vaccinées.
Remarques générales sur les études :
Il n’est pas surprenant que les premières études épidémiologiques sur la population ne fournissent pas des résultats aussi clairs et tranchés que des études cliniques en double aveugle. D’où les hauts les bas, les significatifs et les non significatifs, … Il est par contre intéressant de constater que ces premières études de terrain permettent de confirmer en partie les résultats des études cliniques.
« Mais ça veut dire quoi 50% d’infections en moins après vaccination ? » :
Attention, 50 % pour qui ? Pour les vaccinées ou pour toutes les filles ? Parce que pour les vaccinées, c’est bien plus (70-80% après une dose). Actuellement, en tenant compte du dépistage par frottis tel que réalisé (avec 60 % de femmes vraiment suivies correctement), on est à 6 cancers du col pour 1000 femmes. Sans frottis, on serait donc à 10-20 cancers pour 1000 femmes. C’est la notion de « lifetime risk » (il est de 10 % pour le cancer du sein par exemple). L’efficacité du vaccin sur les souches 16/18 après trois doses est très élevée (études cliniques) et ces souches comptent pour 70 % des cancers. On s’attend donc à une réduction de 6 à 2 cancers pour 1000 femmes vaccinées 3 doses. 4 cancers évités pour 1000 femmes, ou 40 pour 10000…
« En terme de coût pour la santé publique, à 350 euros les 3 doses » :
Je vous laisse calculer le coût d’une vie de frottis à réaliser tous les 3 ans, vous verrez qu’on est au même ordre de grandeur qu’une vaccination en 3 doses. Pourtant personne ne remet en cause l’utilité des frottis au prétexte de leur coût.
« pour une maladie non épidémique » :
Les infections par HPV ne procèdent par par épidémies. Pire, elles sont endémiques ! C’est pas un truc qu’on observe une fois de temps en temps dans la population. C’est là tout le temps, ça circule encore et encore, avec un réservoir alimenté par tous les jeunes gens qui débutent leur vie sexuelle.
« qui se dépiste bien par les frottis est raisonnable ? » :
Les frottis, comme tout dépistage, ont leur lots de faux positifs et de faux négatifs. De plus, ils sont une prévention dite secondaire, et n’évite pas les interventions comme les conisations en cas de lésions avancées, qui ont également un coût financier et moral. Ils sont néanmoins indispensables, et il n’est pas raisonnable d’opposer vaccin et frottis, qui se complètent fort bien l’un l’autre.
Bonjour Julie ! Merci d’avoir pris la peine d’apporter ton analyse sur les études des vaccins HPV !
A propos de votre calcul sur l’incidence des cancers, je comprends bien la démarche est la logique. Nous sommes d’accord qu’on est sur un raisonnement théorique et que selon votre calcul, nous aurions effectivement 40 cancers de moins sur 10.000 femmes vaccinées si l’efficacité du vaccin était de 100%.
Malheureusement, l’efficacité démontrée du vaccin d’après les études scientifiques tablent plutôt sur 70%. Nous aurions donc en moyenne 30% des cancers du col de l’utérus déclenchés par les génotypes 16 et 18 qui passeraient les mailles de la vaccination.
D’autre part, j’aimerais porter votre attention sur le fait qu’effectivement, la vaccination contre les génotypes 16 et 18 pourrait réduire l’incidence des cancers mais nous ignorons si cette vaccination très marginale (seulement 4 génotypes sur 100) ne vas pas perturber l’équilibre écologique des autres HPV, et par exemple, augmenter l’incidence des cancers des autres HPV à haut risque oncogène. Nous n’en savons strictement rien, et c’est bien ce que semble indiquer certaines études décrites dans cet article.
Egalement en défaveur de cette vaccination, quelle est l’efficacité au-delà de 5 ans ? Pour le moment, nous n’en savons rien non plus. Le recul est bien trop faible. Est-ce que l’immunité est conservée au bout de 7 ou 10 ans ? Faut-il une énième dose en rappel ? Là aussi, le doute plane sur l’efficacité (que l’on peut encore revoir à la baisse).
Je peux aussi rajouter une interrogation sur le nombre de femmes qui, une fois vaccinées, pourraient penser à tord être protégées contre le cancer du col et ne réaliseront plus de frottis, et pourraient alors augmenter l’incidence des cancers du col.
Au final, tous ces points sont là principalement pour mettre en avant le bénéfice théorique très bancale de cette vaccination sur une maladie, qui au final, n’est pas du tout une priorité en terme de santé publique.
A propos de ton point sur cette maladie endémique, je suis d’accord avec toi. Mais j’aimerais te poser la question de en quoi est-ce forcément pire ? Je veux dire par là que nous avons des infections aux HPV ultra courantes, et qui possèdent de surcroît un taux de rémission spontané extrêmement élevé. Le fait que les HPV soit endémiques aux Hommes, ne fait pas d’eux une maladie gravissime. La preuve est en par l’épidémiologie de cette maladie qui la place loin dans le classement des maladies mortelles en France et chez les Femmes. Je pense donc sincèrement, au vu de la clairance virale très élevée des infections HPV, que cet argument est un poil alarmiste.
A propos de ton point sur le coût des frottis, tu as parfaitement raison de le préciser, j’aurais moi-même dû en parler. Il se trouve que le suivi d’une femme de 25 à 65 ans, à raison de 13 frottis par femme et pour un coût d’environ 50 euros (les chiffres officiels d’une consultation en cabinet de gynécologie, d’un prélèvement et d’une lecture par un autre spécialiste), cela reviendrait à 650 euros, donc plus cher que les 3 doses de Gardasil.
On peut donc comparer et critiquer les deux méthodes. Mais jusqu’à présent, le frottis s’avère plus efficace que la vaccination et sans effet secondaire. Après, je reste absolument d’accord avec toi que ce sont deux méthodes complémentaires.
Je serais personnellement beaucoup plus favorable à cette vaccination si elle englobait tous les génotypes à haut risque (au moins 14).
Je tiens tout de même à préciser que nous n’avons toujours pas la preuve que cette campagne de vaccination réduira bien la prévalence des cancers du col en France. Il faut vacciner pour le vérifier, et cela ressemble beaucoup à des tests de laboratoire sur des cobayes à l’échelle d’une population.
@Jérémy
« nous n’avons toujours pas la preuve que cette campagne de vaccination réduira bien la prévalence des cancers du col en France. »
« cela ressemble beaucoup à des tests de laboratoire sur des cobayes à l’échelle d’une population»
Le seul critère de mise sur le marché d’un médicament (brevetable) ou d’un vaccin est la rentabilité.
Le laboratoire avait réussi sa campagne publicitaire d’intoxication de l’opinion publique pour le vaccin contre la grippe qui risque de tuer des millions de personnes si on ne procédait pas à une vaccination massive de la population mondiale.
« La grippe est une infection respiratoire aiguë très contagieuse, provoquée par un virus. Souvent considérée comme une maladie bénigne, elle est pourtant RESPONSABLE DE NOMBREUX DÉCÈS, en particulier aux âges extrêmes de la vie et chez les personnes atteintes de certaines maladies respiratoires, cardiovasculaires, rénales ou encore de diabète »
http://sante.lefigaro.fr/mieux-etre/vaccination-depistage/vaccination-contre-grippe/pourquoi-se-faire-vacciner
Quand on est vieux et malade on risque évidemment de mourir. Il est vrai qu’une mauvaise grippe peut être fatale dans ce cas, mais on fini toujours par mourir de quelque chose, surtout si on est déjà très malade.
L’intérêt des vaccins est que cela permet de vendre très chers une énorme quantité de « médicaments » ou vaccins à des personnes en bonne santé.
Il n’y a aucun recours possible contre le laboratoire, car il est impossible de prouver que le médicament ou le vaccin est la cause d’un décès ou de complications graves, surtout chez un enfant encore en bonne santé.
La quasi totalité des produits chimiques appelés « médicaments » sont inefficaces, « inutiles et dangereux » et donc il est plus rentable de vendre ces produits industriels à des personnes qui ne sont pas malades et plus nombreuses que les personnes âgées et malades.
« La France détruit ses vaccins contre la grippe A
Par Tony David publié le 12/09/2011
En novembre, les dernières doses de vaccin contre le H1N1 seront incinérées. Au final 19 millions de doses ont été détruites, pour un coût total d’achat et de destruction- d’environ 400 millions d’euros. »
« Le ministère de la santé veut aujourd’hui tirer les leçons de ce gâchis: »
http://www.lexpress.fr/actualite/societe/sante/la-france-detruit-ses-vaccins-contre-la-grippe-a_1029142.html
Les gouvernements changent mais les ministres de la santé ne s’intéressent qu’à leur portefeuille.
Le gaspillage de l’argent publique et la santé des enfants qui sont traités comme des cobayes sans défense ne sont pas leur priorité.
Il est plus important de permettre aux lobbies d’engranger des milliards de dollars, d’euro ou de n’importe quoi en rendant la vaccination obligatoire.
Une simple signature sur un bout de papier suffit à condamner tous les enfants de France à un traitement onéreux inutile.
Révoltant ?
« Je n’ai jamais rencontré de parents rebelles parmi les parents d’élèves des classes de mes enfants….des moutons oui…..les jeunes parents sont tout aussi aveugles, peu osent fronder. Comment voulez vous qu’une jeune maman de 20/30 ans s’élève…contre le directeur de l’école, de la crèche, ses parents, ses beaux parents , la société… »
http://www.dur-a-avaler.com/vaccins-hpv-contre-papillomavirus-petition-joyeux-sante-nature-innovation-ipsn-rapport-hcsp/#comment-19377
Bonjour M. Grossbouff,
http://www.dur-a-avaler.com/vaccins-hpv-contre-papillomavirus-petition-joyeux-sante-nature-innovation-ipsn-rapport-hcsp/#comment-19322
Le sujet traité par Jérémy concerne la vaccination contre les Papillomavirus.
« Dans un article précédent, je (Jérémy) vous ai exposé la polémique qui sévit actuellement contre les vaccins HPV (Human Papilloma Virus), mais surtout contre le dernier rapport émis par le Haut Conseil de Santé Publique (HCSP) qui recommande une vaccination dès 9 ans à l’école. »
Il ne s’agit nullement d’une campagne contre la vaccination, ni de remettre en cause le principe de la vaccination pour des maladies mortelles.
Par contre rendre obligatoire un vaccin pour lequel « Il n’y a absolument aucune preuve à l’heure actuelle que les vaccins HPV protègent contre le cancer du col de l’utérus. La
soi-disant protection est supposée. »
http://www.dur-a-avaler.com/vaccins-hpv-contre-papillomavirus-petition-joyeux-sante-nature-innovation-ipsn-rapport-hcsp/#comment-19132
est abusif et n’est destiné qu’à servir les intérêts des laboratoires pharmaceutiques au détriment de la santé des enfants scolarisés en France.
En France les vaccinations OBLIGATOIRES sont les suivantes :
– contre la diphtérie et le tétanos : seule la primo vaccination avec le 1er rappel à 11 mois est obligatoire ;
– contre la poliomyélite : la primo vaccination et les rappels sont obligatoires jusqu’à l’âge de 13 ans ;
– contre la fièvre jaune : pour toutes les personnes résidant en Guyane.
http://vosdroits.service-public.fr/particuliers/F724.xhtml
Seuls trois vaccins sont obligatoires en France. L’imposition de tout autre vaccin est illégale.
http://www.wikistrike.com/article-seuls-trois-vaccins-sont-obligatoires-en-france-l-imposition-de-tout-autre-vaccin-est-illegale-118787357.html
Les vaccinations RECOMMANDÉES concernent :
– les maladies telles que la coqueluche, la rubéole, la rougeole, les oreillons, la varicelle,
– les infections invasives à haemophilus influenza b, à pneumocoque, à méningocoque C,
– les hépatites B et A (pour les professionnels exposés à un risque de contamination).
– les infections à papillomavirus humains (pour les jeunes filles entre 11 et 14 ans),
Le vaccin contre la grippe est facultatif mais conseillé.
Les infections à papillomavirus humains :
« 90% des infections dû aux HPV se résorbent d’elle-même dans les deux ans et tous les stades d’évolutions des lésions précancéreuses (CIN 1 à 3) peuvent régresser spontanément (dans 32 à 57% des cas), au final, une infection aux HPV à moins de 0,2% de chance d’évoluer en cancer invasif »
http://www.dur-a-avaler.com/vaccins-hpv-contre-papillomavirus-petition-joyeux-sante-nature-innovation-ipsn-rapport-hcsp/#comment-19132
Les infections dues aux HPV ne sont pas plus mortelles que la grippe et le cancer du col est un cancer localisé qui ne met pas la vie de la femme en danger.
Rendre obligatoire les vaccins HPV pour lesquels il n’y a absolument aucune preuve à l’heure actuelle qu’ils protègent contre le cancer du col de l’utérus est un abus de pouvoir des laboratoires pharmaceutiques.
Cette action serait même illégale et passible de poursuites.
« A propos de votre calcul sur l’incidence des cancers, je comprends bien la démarche est la logique. »
Dans ce cas, vous serez d’accord pour admettre qu’il y a l’un ou l’autre problème de logique dans votre calcul.
1) Vous partez d’une prévalence de 47 % pour arriver à 9 cancers pour 10000 femmes. Or, cette prévalence n’est pas une « prévalence à vie », c’est la prévalence pour les femmes de l’étude à un moment donné de leur vie. Ces femmes poursuivent leur vie, et en particulier leur vie sexuelle, une fois l’étude terminée. Partir de ce chiffre n’est donc pas une bonne méthode. C’est la raison pour laquelle vous n’arrivez pas à reproduire les observations qui n’ont rien de théoriques, qui sont qu’actuellement, 6 femmes pour 1000 sont concernées par ce cancer au cours de leur vie, et que 10-20 le seraient en l’absence des frottis (vous devriez donc arriver à 100-200 cancers du col pour 10000 femmes, vous en êtes loin avec 9/10000).
2) La probabilité de clairance virale n’est pas la même pour tous les HPV (ex: http://aje.oxfordjournals.org/content/158/5/486.full). C’est d’ailleurs pour cela que certains sont plus oncogènes que d’autres… La proportion de HPV 16 et 18 impliqués dans ces cancers est connue, et elle est de 70 %. Ce n’est pas de la théorie.
3) Les 27 % de diminution pour les HPV à haut risque constituent une estimation brute que vous faites à partir du tableau 2 de l’article. L’OR ajusté est donné dans le tableau 3 et est de 0,55 ce qui correspond en fait à une diminution de 45 %. Par ailleurs, cette diminution vaut pour l’entièreté de la population post-vaccinale, qui n’est pas vaccinée dans son entièreté. L’OR pour les vaccinées est de 0,5, tandis que celui des non vaccinées n’est pas significativement différent de 1. Enfin, puisqu’on sait quelle proportion de cancers est due aux HPV 16 et 18, autant s’intéresser directement à leur diminution. Ce qui s’en rapproche le plus dans le tableau est l’OR pour les HPV vaccinaux chez les vaccinées qui est de 0,11 ; indiquant une diminution de 89 %.
Donc si vous vouliez partir de cette étude et des observations sur l’épidémiologie des infections, et sans tenir compte des frottis (puisque vous n’en avez pas tenu compte dans votre estimation), il vous faudrait conclure que le vaccin, si il est administré à 10000 jeunes filles avant le début de leur vie sexuelle, leur permettra d’éviter 100-200*0,70*0,89=60-120 cancers. Je préfère pour ma part partir de la situation actuelle : 60*0,70*0,89=40 cancers évités.
Les 89 % d’efficacité correspondent ici à une efficacité pour entre 1 et 3 doses sur une population où certaines filles vaccinées n’étaient peut-être plus vierges. Vous pouvez encore aller un peu plus loin, cad jusqu’aux résultat des études cliniques qui sont de presque 100 % pour les populations per protocol pour imaginer ce qu’il serait possible d’obtenir si les filles étaient vaccinées correctement.
« nous ignorons si cette vaccination très marginale (seulement 4 génotypes sur 100) ne vas pas perturber l’équilibre écologique des autres HPV »
Il est assez étrange de qualifier de marginale une vaccination qui couvre les souches responsables de 70 % des cancers du col et de 90 % des condylomes, au prétexte qu’il existe plus d’une centaine de souches. Quand vous prenez une assurance, vous vous concentrez sur les risques les plus susceptibles de se réaliser, pas sur l’ensemble des risques non ?
La perturbation de l’équilibre écologique est considérée comme peu probable, car les HPV ne se disputent pas la niche écologique (d’où la possibilité d’infections multiples simultanées). C’est quelque chose à surveiller, mais pas un motif d’immobilisme.
«quelle est l’efficacité au-delà de 5 ans ?»
Effectivement, les études cliniques étaient limitées dans le temps et le chiffre de 5 ans a été annoncé. Mais il est repris de façon déformée… Au bout de 5 ans, l’efficacité était toujours très bonne. Les taux d’anticorps ne disparaissant pas du jour au lendemain, il est évident que l’efficacité est de plus 5 ans. D’ailleurs, je suis certaine que si vous creusez un peu, vous trouverez de nouvelles estimations de cette durée, puisque le vaccin est sur le marché depuis maintenant 8 ans.
« Je peux aussi rajouter une interrogation sur le nombre de femmes qui, une fois vaccinées, pourraient penser à tord être protégées contre le cancer du col et ne réaliseront plus de frottis, et pourraient alors augmenter l’incidence des cancers du col. »
Le risque existe. Mais c’est le rôle du prescripteur d’expliquer que le vaccin ne dispense pas des frottis, de la même façon qu’il explique que la pilule ne dispense pas du préservatif… de la même façon que les airbags ne dispense pas du port de la ceinture, etc…
« sur une maladie, qui au final, n’est pas du tout une priorité en terme de santé publique. »
Si cette maladie n’était pas une priorité en terme de santé publique, pourquoi encourager les frottis alors ? Je constate très souvent cette distorsion dans la perception du problème selon la solution envisagée (si vaccin, alors y a pas de problèmes à résoudre. Si frottis, alors là faut foncer ma bonne dame…).
« A propos de ton point sur cette maladie endémique, je suis d’accord avec toi. Mais j’aimerais te poser la question de en quoi est-ce forcément pire ? »
Parce que les virus peuvent atteindre tout le monde et pas seulement une partie de la population de temps en temps, au petit bonheur la chance… Virus qui sans contrôle impliqueraient 100-200 cancers du col pour 10000 femmes… ça ne me semble pas être quelque chose de bénin. Mais chacun a droit à la subjectivité.
« On peut donc comparer et critiquer les deux méthodes. Mais jusqu’à présent, le frottis s’avère plus efficace que la vaccination et sans effet secondaire. »
Il ne faut pas oublier que si un souci est détecté avec les frottis, il faudra intervenir. Ce sont les effets secondaires et les inconvénients (physiques et psychologiques) de ces interventions qu’il faut aussi mettre dans la balance.
« Je serais personnellement beaucoup plus favorable à cette vaccination si elle englobait tous les génotypes à haut risque (au moins 14). »
C’est une évidence qui doit être partagée par le plus grand nombre ;)
@ Julie:
Merci encore pour ce commentaire.
C’est en revérifiant tous ces calculs de probabilité que je me suis rendu que tu surestimais extrêmement l’incidence des cancers du col de l’utérus en France.
D’après les chiffres officiels de l’INVS, l’incidence est de 8 cancers pour 100.000 femmes !
D’après mes calculs théoriques, sur la base de l’étude de Tabarzi, je trouve 9 cancers pour 10.000 femmes, soit 90 cancers pour 100.000 femmes ! Je suis donc bien au-dessus des statistiques nationales.
Quoiqu’il en soit. Je vais donc reprendre la base de mon calcul sur les statistiques nationales.
Ainsi, 8 cancers touchent 100.000 femmes. En théorie, 70% de ces cancers seraient attribuables aux génotypes 16 et 18, soit 5 à 6 cancers.
Donc, si l’on vaccine 100.000 femmes, avec le prix des 3 doses, cela revient à dépenser 5 ou 6 millions d’euros pour éviter un seul cancer. Et je le rappelle, nous ne savons s’il entraînera la mort ou pas de la personne. Si l’on compare ces 5 millions d’euros, contre
A partir de ce moment, sachant que nous n’avons pour le moment aucune idée de l’efficacité réelle de ce vaccin sur l’incidence des cancers du col, qu’il y a un certains nombres d’effets secondaires graves reportés (je rappelle que l’innocuité du vaccin a été établie sur la base d’études financées par les laboratoires pharmaceutiques, en terme d’indépendance, on fait mieux, largement mieux), sachant que si je prend l’efficacité du vaccin à 89% on tombe bien à 5 cancers évités pour 300.000 doses à 350 euros, sachant que le vaccin ne protège pas contre tous les HPV (30% à haut risque oncogène persistent), sachant que ce cancer n’est que le 15ème en terme d’incidence…
Alors oui, on peut décemment remettre en question cette vaccination.
Cette maladie n’est pas une priorité en terme de santé publique, je persiste et signe. C’est l’épidémiologie qui le confirme. Et il apparaît tellement évident qu’il faille améliorer la couverture par frottis car sans effet secondaire et plus efficace que la vaccination, qui je le rappelle n’a pas encore fait ces preuves !
Le fait que le frottis détecte les lésions précancéreuses et entraîne l’engagement d’opération médicale lourde et coûteuse ne le rend pas responsable de la maladie. Le frottis est simplement là pour détecter un problème, qui serait là de toute façon, et permet je suis sûr d’alléger les dépenses de santé en évitant des traitements de cancers invasifs par exemple très coûteux.
Je trouve qu’il est facile de dramatiser la situation endémique des HPV en France alors que la clairance virale totale et moyenne est extrêmement élevée. Avec des si on pourrait refaire le monde, et je ne vois pas pourquoi du jour au lendemain le système de santé arrêtera les contrôles par dépistages. Les infections aux HPV sont extrêmement courante et se résorbent très majoritairement d’elles mêmes.
Pour terminer, même si il y a tellement à dire, ma dernière phrase parlant des 14 génotypes sur un hypothétique vaccin met en avant les limitations majeures du Gardasil, et les nombreuses interrogations qui planent sur son efficacité réelle, et notamment à long terme, sur les effets secondaires à long terme également, et qu’il extrêmement sage de remettre en question cette vaccination, surtout en France.
Peut-être que l’avenir nous apportera des éléments favorables sur ces vaccins, mais à ce jour, il peut-être évité avec une démarche de dépistage responsable notamment (mais aussi en contrôlant d’autres facteurs de risques comme le tabagisme, la malbouffe, etc.)
Bonjour
merci pour cet article et les commentaires, de qualité.
Je suis médecin généraliste et épidémiologiste et assez concerné sur les deux plans par la possible utilité du vaccin. Je n’ai pas encore tout lu en détail mais sans être foncièrement anti vaccin (je reconnais par exemple de l’efficacité du DTP de l’haemophilus, de l’anti amarile et d’autres) je crois que l’on peut se poser des sérieuses questions sur :
L’efficacité réelle sur le cancer
L’efficience de la vaccination de masse.
juste une citation
<>
Je rappelle que pour le prevenar 7 l’efficacité a été merveilleuse le temps que la population phénotypale change et que les US se retrouvent avec une recrudescence d’infection à pneumocoques plus raves (rapide et létales) ce qui sur le plan évolution peut se comprendre (ce qui vous tue rapidement se diffuse moins). On est alors passé au Prevenar 13 qui pour le moment se tient bien en terme d’efficacité (je reste néanmoins sceptique sur l’efficience même si je l’injecte quotidiennement).
“C’est en revérifiant tous ces calculs de probabilité que je me suis rendu que tu surestimais extrêmement l’incidence des cancers du col de l’utérus en France. D’après les chiffres officiels de l’INVS, l’incidence est de 8 cancers pour
100.000 femmes !”
Vous confondez la notion d’incidence annuelle et de risque à vie… Je ne surestime certainement pas le risque à vie qui est de 6/1000 actuellement en France
Lisez ici en page 8 : http://www.pasteur.fr/ip/resource/filecenter/document/01s-00004i-00u/cancer-col-uterus-2008.pdf
ou là: http://lesdonnees.e-cancer.fr/les-indicateurs/1-types-cancer/13-cancer-col-uterus/12-epidemiologie-cancer-col-uterus-france-metropolitaine-essentiel/22-risque-de-developper-un-cancer-du-col-de-luterus-entre-0-et-74-ans-en-france-c.html)
« Je serais personnellement beaucoup plus favorable à cette vaccination si elle englobait tous les génotypes à haut risque (au moins 14). »
Surveillez donc l’arrivé possible du « gardasil-9 » dans les mois ou années à venir… :
http://www.skepticalraptor.com/skepticalraptorblog.php/powerful-cancer-preventing-gardasil-vaccine-cleared-fda/
France 5 a diffusé mardi 10/02/15 un excellent documentaire sur Merck fabricant du gardasil et en parle longuement à la fin (1h10 en tout)
http://www.france5.fr/emission/medicaments-sous-influence/diffusion-du-10-02-2015-20h40
Tout est dit : Gardasil risque d’être le nouveau Vioxx, la corruption massive des politiques pour l’imposer mondialement même là ou cela n’a pas de sens…
votre démonstration est sidérante !
je vous propose d’attendre 20 ans pour voir l’impact ou pas du vaccin sur les cancers du col. au pire quelques milliers de femmes dans le monde auront un cancer du col qu’elles auraient pu éviter…
vous insister très lourdement sur les conflits d’intérêts, c’est tout à votre honneur et je suis d’accord avec vous… mais, vous perdez toute crédibilté en citant le bon pr joyeux qui est au sommet des conflits d’intérêts avec tous ses potes “natu ô pattes”. renseignez-vous, fouillez un peu plus de ce côté-là aussi ! ne soyez pas sectaire et à charge !
d’un côté les méchants labos pharmaceutiques et de l’autre les gentils amis de l’homme et de la nature… le monde des bisounours !